
Études de biodisponibilité
Consulter les études comparatives de biodisponibilité chez des sujets à jeun et non à jeun
Étude comparative de biodisponibilité à dose orale unique (1 x 18 mg)
Étude comparative de biodisponibilité à dose orale unique (1 x 18 mg) menée chez des sujets à jeun et non à jeun
Profil de la concentration moyenne – temps du méthylphénidate après l’administration de la formule testée (traitement A) et du produit de référence (traitement B)1,2,†
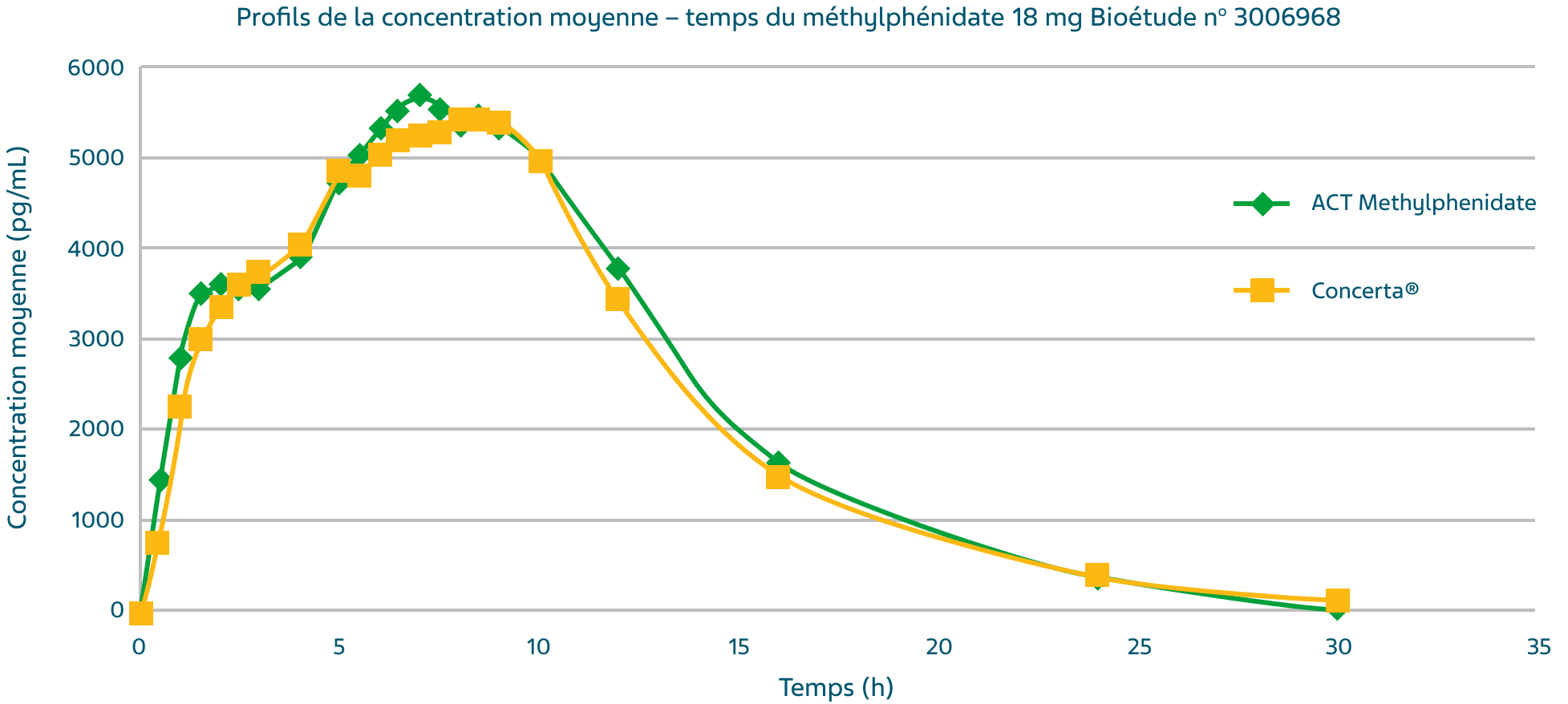
Étude comparative de biodisponibilité à dose orale unique (1 x 18 mg) menée chez des sujets à jeun
Profil de la concentration moyenne – temps du méthylphénidate après l’administration de la formule testée (traitement A) et du produit de référence (traitement B)1,3,‡
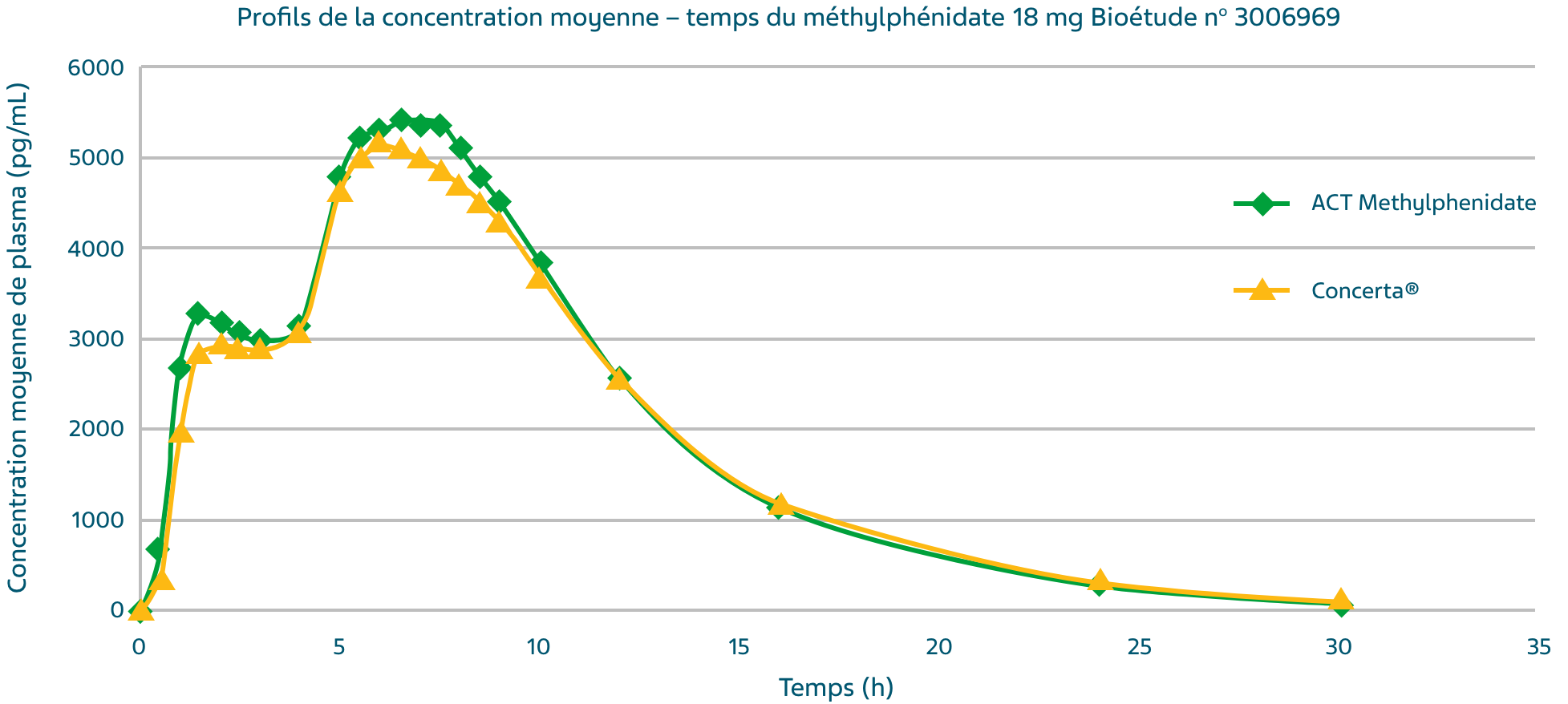
†Une étude croisée portant sur deux traitements à dose unique administrés sur deux périodes avec inversion de traitement a été menée chez des adultes en bonne santé et non à jeun dans le but d’évaluer la bioéquivalence des comprimés de 18 mg de chlorhydrate de méthylphénidate à libération prolongée (Teva Canada Limitée) et de comprimés de 18 mg de Concerta® (chlorhydrate de méthylphénidate) à libération prolongée de Janssen Inc., Canada.
‡Une étude croisée portant sur deux traitements à dose unique administrés sur deux périodes avec inversion de traitement a été menée chez des adultes en bonne santé et à jeun dans le but d’évaluer la bioéquivalence des comprimés de 18 mg de chlorhydrate de méthylphénidate à libération prolongée (Teva Canada Limitée) et de comprimés de 18 mg de Concerta® (chlorhydrate de méthylphénidate) à libération prolongée de Janssen Inc., Canada.
Étude comparative de biodisponibilité à dose orale unique (1 x 54 mg)
Étude comparative de biodisponibilité à dose orale unique (1 x 54 mg) menée chez des sujets à jeun et no à jeun
Profil de la concentration moyenne – temps du méthylphénidate après l’administration de la formule testée (traitement A) et du produit de référence (traitement B)1,4,§
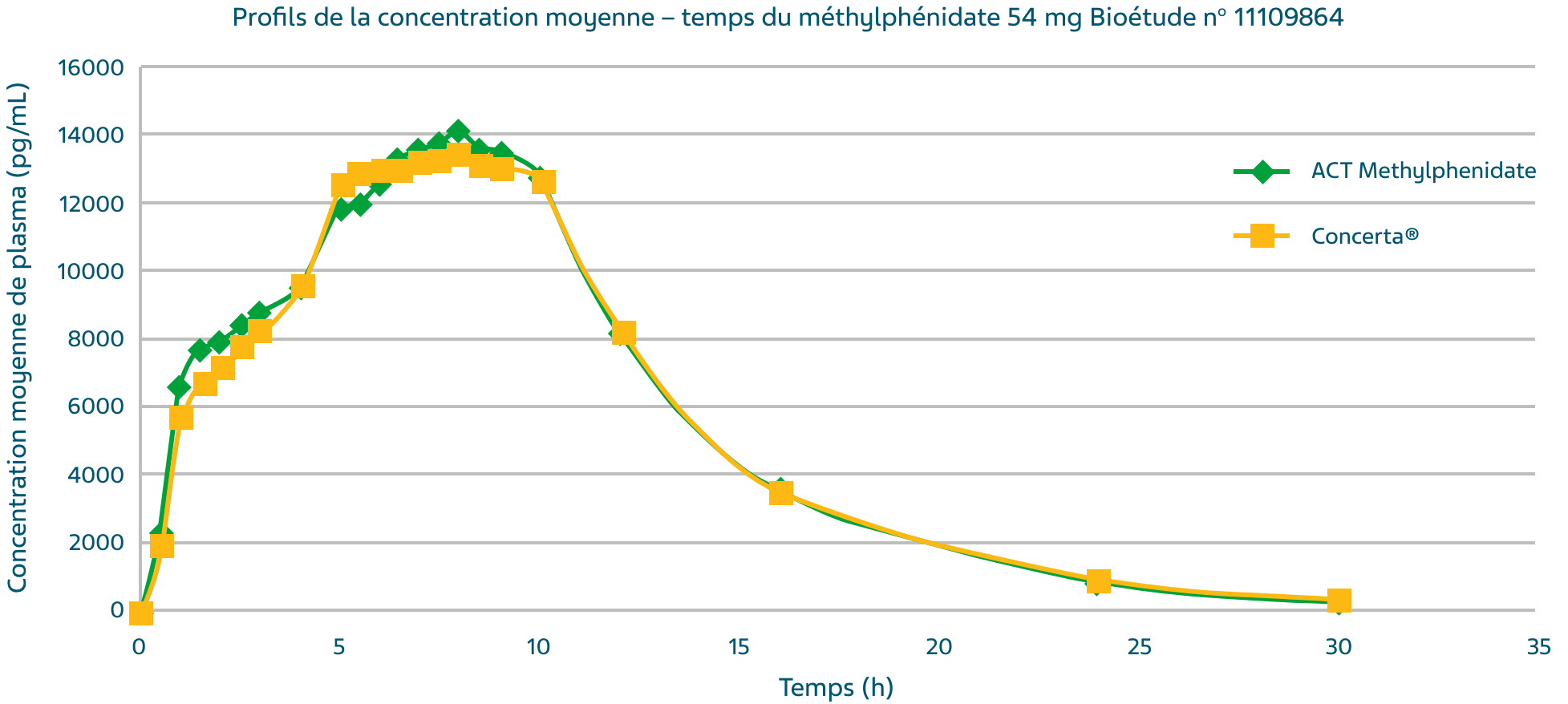
Étude de comparative de biodisponibilité à dose orale unique (1 x 54 mg) menée chez des sujets à jeun
Profil de la concentration moyenne – temps du méthylphénidate après l’administration de la formule testée (traitement A) et du produit de référence (traitement B)1,5,#
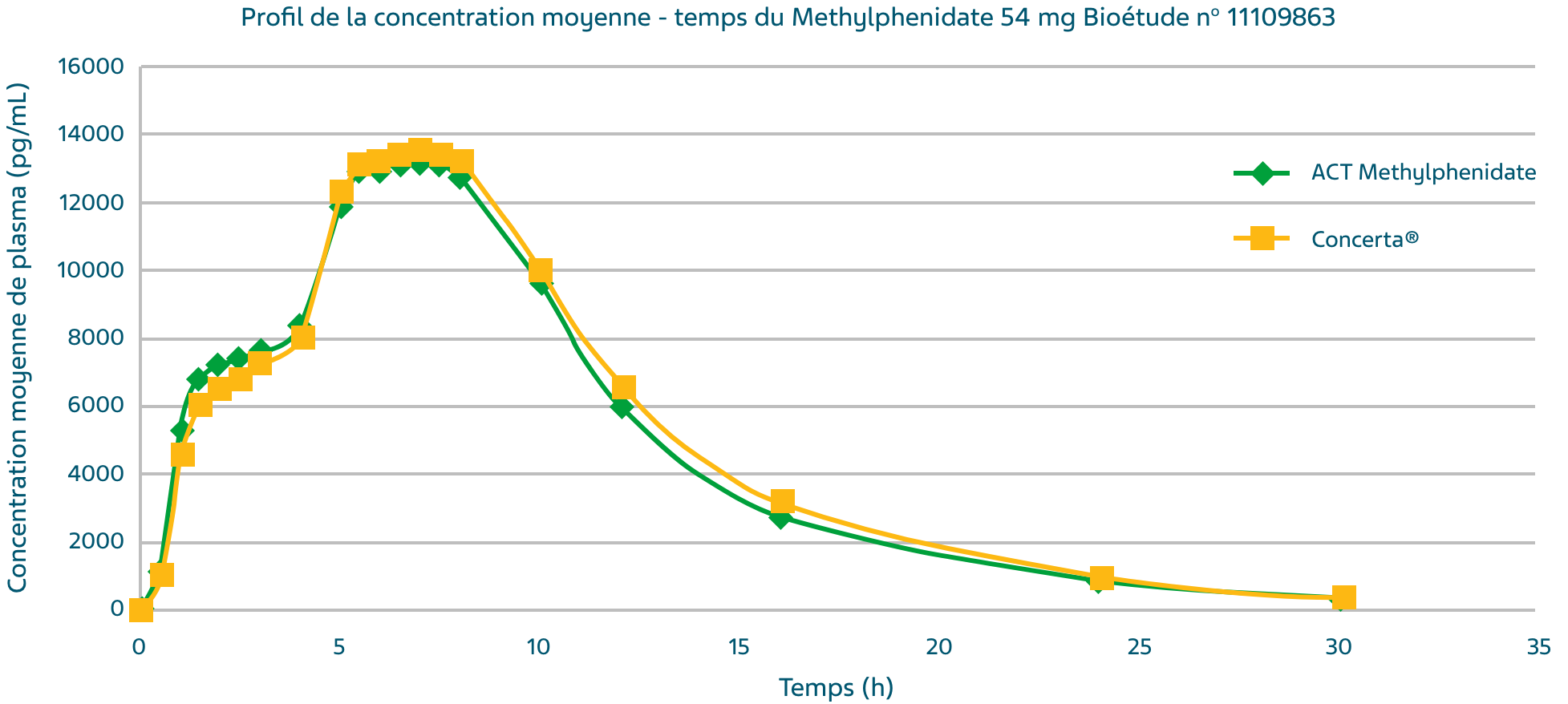
§Une étude croisée portant sur deux traitements à dose unique administrés sur deux périodes avec inversion de traitement a été menée chez des adultes en bonne santé et non à jeun dans le but d’évaluer la bioéquivalence des comprimés de 18 mg de chlorhydrate de méthylphénidate à libération prolongée (Teva Canada Limitée) et de comprimés de 54 mg de Concerta® (chlorhydrate de méthylphénidate) à libération prolongée de Janssen Inc., Canada.
#Une étude croisée portant sur deux traitements à dose unique administrés sur deux périodes avec inversion de traitement a été menée chez des adultes en bonne santé et à jeun dans le but d’évaluer la bioéquivalence des comprimés de 18 mg de chlorhydrate de méthylphénidate à libération prolongée (Teva Canada Limitée) et de comprimés de 54 mg de Concerta® (chlorhydrate de méthylphénidate) à libération prolongée de Janssen Inc., Canada.
References:
- Teva Canada Limitée. Monographie du produit ACT Methylphenidate ER. Le 14 février 2024.
- Données dans le fichier. Bioétude no 3006968.
- Données dans le fichier. Bioétude no 3006969.
- Données dans le fichier. Bioétude no 11109864.
- Données dans le fichier. Bioétude no 11109863.
Bioéquivalence établie à Concerta®
La formule à libération modifiée d’ACT Methylphenidate ER a été mise au point pour offrir un profil de libération du méthylphénidate identique à celui de Concerta®.
Regarder la vidéo des études comparatives de biodisponibilité.
Pour en apprendre plus au sujet d’ACT Methylphenidate ER



